
Conţinut
- Cancer de sân ereditar
- Mutații genice non-BRCA
- Cancerul de sân și testarea genetică
- Sprijin pentru cancerul de sân ereditar
În plus față de mutațiile genelor BRCA1 și BRCA2, unele dintre acestea includ mutații în ATM, PALB2, PTEN, CDH1, CHEK2, TP53, STK11, PMS2 și multe altele. Să vedem cât de importante sunt aceste mutații non-BRCA1 / BRCA2 în cancerul de sân familial și câteva dintre caracteristicile celor mai frecvent găsite.
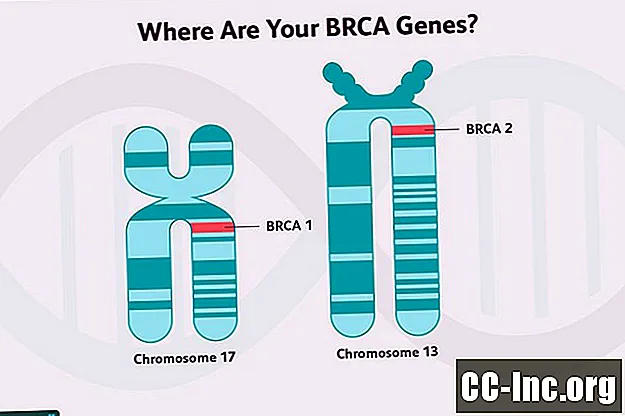
Cancer de sân ereditar
În prezent, se crede că 5 la 10 la sută din cancerele de sân sunt genetice sau familiale (deși acest număr se poate schimba pe măsură ce aflăm mai multe), dar nu toate aceste tipuri de cancer se datorează mutațiilor BRCA.
Cel mult, 29% (și probabil mult mai puține) cancerele de sân ereditare sunt pozitive pentru mutațiile genei BRCA1 sau BRCA2 și mulți oameni urmăresc testarea celorlalte modificări genetice cunoscute.
Întrucât știința din spatele cancerului ereditar provoacă foarte multă anxietate, ca să nu vorbim despre confuzie și incompletă, este util să începem prin a vorbi despre biologia mutațiilor genetice și despre modul în care aceste modificări ale ADN-ului joacă un rol în dezvoltarea cancerului.
Mutații genetice moștenite vs.
Când vorbim despre mutații, este important să se facă distincția între mutațiile genetice moștenite și cele dobândite.
Mutațiile genice dobândite sau somatice au primit multă atenție în ultimii ani, deoarece aceste mutații provoacă modificări care determină creșterea cancerului. Terapiile vizate, medicamente care vizează căi specifice legate de aceste modificări, au îmbunătățit semnificativ tratamentul unor tipuri de cancer precum cancerul pulmonar.
Mutațiile dobândite, totuși, nu sunt prezente de la naștere, ci mai degrabă, se formează oricând după naștere, în procesul de transformare a unei celule în celule canceroase. Aceste mutații afectează doar unele celule din corp. Ele nu sunt moștenite de la un părinte, ci mai degrabă „dobândite”, deoarece ADN-ul din celule este expus la deteriorarea mediului sau ca urmare a proceselor metabolice normale ale corpului.
Mutațiile moștenite sau germinale, în schimb, sunt modificări genetice cu care oamenii se nasc și care sunt transmise de la unul sau de la ambii părinți. Aceste mutații afectează toate celulele corpului. Aceste mutații moștenite (și alte modificări genetice) pot crește șansele ca o persoană să dezvolte cancer și să explice ceea ce este cunoscut sub numele de cancer de sân ereditar sau familial.
Mutații genetice ereditare (germinale) vs. dobândite (somatice)Cum cresc mutațiile genetice ereditare riscul de cancer?
Mulți oameni se întreabă cum exact o genă anormală sau combinații de gene ar putea duce la apariția cancerului de sân, iar o scurtă discuție despre biologie este utilă pentru a înțelege multe dintre întrebări, precum de ce nu toți cei care au aceste mutații dezvoltă cancer.
ADN-ul nostru este un plan sau cod care este utilizat pentru fabricarea proteinelor. Atunci când harta sau codul sunt greșite (cum ar fi „litere” într-o anumită genă), acesta oferă direcții greșite pentru sintetizarea unei proteine. Proteina anormală este apoi incapabilă să-și îndeplinească sarcina obișnuită. Nu toate mutațiile genice cresc riscul de cancer și, de fapt, majoritatea nu. Mutațiile genelor responsabile de creșterea și divizarea celulelor sau „mutațiile conducătorului auto” sunt cele care determină creșterea cancerelor. Există două tipuri majore de gene care, atunci când sunt mutate, pot duce la creșterea necontrolată cunoscută sub numele de cancer: oncogene și gene supresoare tumorale.
Mai multe dintre genele asociate cu un risc mai mare de cancer mamar sunt gene supresoare tumorale. Aceste gene codifică proteinele care funcționează pentru a repara deteriorarea ADN-ului din celule (daune cauzate de toxinele din mediu sau procesele metabolice normale din celule), servesc la eliminarea celulelor care nu pot fi reparate sau reglează creșterea în alte moduri. Genele BRCA1 și BRCA2 sunt gene supresoare tumorale.
Multe dintre aceste gene sunt autosomale recesive, ceea ce înseamnă că fiecare persoană moștenește o copie a genei de la fiecare părinte, iar ambele copii trebuie mutate pentru a crește riscul de cancer. Simplist, aceasta înseamnă că o combinație de factori genetici și de mediu (o mutație dobândită în cealaltă genă) trebuie să acționeze împreună pentru a duce la dezvoltarea cancerului. Adăugat la aceasta, de obicei, trebuie să apară mai multe mutații pentru ca o celulă să devină o celulă canceroasă.
Ce înseamnă să ai o predispoziție genetică la cancerPenetrarea genelor
Nu toate mutațiile genetice sau modificările genetice cresc riscul de cancer mamar în același grad și acesta este un concept important pentru oricine are în vedere testarea genetică, mai ales că mulți oameni au auzit de riscul foarte ridicat conferit de mutațiile BRCA. Penetrarea genică este definită ca proporția persoanelor cu mutație care vor experimenta această afecțiune (în acest caz, dezvoltă cancer de sân).
Pentru unele mutații, riscul de cancer mamar este foarte mare. Pentru alții, riscul poate fi crescut doar cu un factor de 1,5. Acest lucru este important de înțeles atunci când vorbim despre posibile opțiuni preventive.
Epigenetica
Un alt concept important, care este important în înțelegerea geneticii și cancerului, deși este prea complex pentru a fi explorat în detaliu aici, este cel al epigeneticii. Am aflat că modificările ADN-ului care nu implică modificări în perechile de baze (nucleotide) sau „literele” care codifică o proteină, pot fi la fel de importante în dezvoltarea cancerului. Cu alte cuvinte, în loc de modificări structurale în coloana vertebrală a ADN-ului, pot exista modificări moleculare care schimbă modul în care mesajul este citit sau exprimat.
Mutații genice non-BRCA
Mutațiile genei BRCA sunt cele mai cunoscute anomalii genetice asociate cu cancerul de sân, dar a fost clar că există femei care sunt predispuse la cancerul de sân pe baza istoricului lor familial, care dau rezultate negative.
Un studiu din 2017 a constatat că mutațiile BRCA au reprezentat doar 9% până la 29% din cancerele de sân ereditare. Chiar și atunci când s-au făcut teste pentru alte 20-40 de mutații cunoscute, totuși, doar 4% până la 11% dintre femei au fost testate pozitiv. Cu alte cuvinte, 64% până la 86% dintre femeile suspectate de cancer mamar ereditar au fost testate negativ atât pentru mutațiile BRCA, cât și pentru 20 până la 40 de persoane.
Cancer de sân non-BRCA1 / BRCA2
Cunoștințele noastre despre mutațiile genetice care cresc riscul de cancer mamar sunt încă incomplete, dar știm acum că există cel puțin 72 de mutații genetice legate de cancerul mamar ereditar. Se consideră că aceste mutații (și altele încă nedescoperite) sunt responsabile de 70% până la 90% din cancerele de sân ereditare care testează negativ pentru mutațiile genei BRCA. Acronimul BRCAX a fost inventat pentru a descrie aceste alte mutații, reprezentând non- BRCA1 BRCA2- cancer de sân familial asociat.
72 Mutații genetice legate de cancerul de sân ereditarAnomaliile genetice de mai jos diferă în ceea ce privește frecvența, cantitatea de risc asociată, tipul de cancer de sân cu care sunt legate și alte tipuri de cancer asociate cu mutațiile.
Majoritatea acestor tipuri de cancer de sân au caracteristici similare (cum ar fi tipul de cancer, starea receptorilor de estrogen și starea HER2) cu tipurile de cancer de sân neereditare sau sporadice, dar există excepții. De exemplu, unele mutații sunt mai puternic asociate cu cancerul de sân triplu negativ, inclusiv mutații în BARD1, BRCA1, BRCA2, PALB2, șiRAD51D.
Variabilitatea în cadrul mutațiilor
Nu toți oamenii care au următoarele mutații genetice sunt la fel. În general, pot exista sute de moduri în care aceste gene sunt mutate. În unele cazuri, gena va produce proteine care suprimă creșterea tumorii, dar proteinele nu vor funcționa la fel de bine ca și proteina normală. Cu alte mutații, este posibil ca proteina să nu fie produsă deloc.
BRCA (O scurtă revizuire pentru comparație)
Mutațiile genei BRCA 1 și mutațiile genei BRCA2 sunt ambele asociate cu un risc crescut de a dezvolta cancer de sân, precum și cu alte tipuri de cancer, deși cele două diferă oarecum în acest risc.
În medie, 72% dintre femeile care suferă de mutații BRCA1 și 69% care au mutat genele BRCA2 vor dezvolta cancer de sân până la vârsta de 80 de ani.
În plus, cancerele de sân asociate cu aceste mutații pot diferi. Cancerele de sân la femeile care suferă de mutații BRCA1 sunt mai susceptibile de a fi triplu negative. Aproximativ 75 la sută sunt receptori estrogeni negativi și, de asemenea, sunt mai puțin susceptibile de a fi HER2 pozitive. De asemenea, sunt mai predispuși să aibă un grad tumoral mai ridicat. Cancerele de sân la femeile cu mutații BRCA2, în schimb, sunt similare cu cancerele la femeile care nu sunt purtătoare ale mutației genei BRCA.
Gen ATM (serină ATM / treonină kinază)
Gena ATM codifică proteinele care ajută la controlul ratei de creștere a celulelor. De asemenea, ajută la repararea celulelor deteriorate (celule care au suferit daune ADN-ului de la toxine) prin activarea enzimelor care repară aceste daune.
Cei care au două copii ale genei mutante au un sindrom autosomal recesiv neobișnuit cunoscut sub numele de ataxie-telangiectazie. Cu ataxia-telangiectazie, proteinele defecte nu numai că măresc riscul de cancer, dar au ca rezultat faptul că unele celule din creier se sting prea repede, rezultând o tulburare neurodegenerativă progresivă.
Persoanele care au o singură copie mutată a genei (aproximativ 1 la sută din populație) au un risc de 20 la 60 la sută pe parcursul vieții de a dezvolta cancer de sân.
Se crede că persoanele care suferă de această mutație sunt predispuse la cancer de sân la o vârstă fragedă, precum și la dezvoltarea cancerului de sân bilateral.
Se recomandă screeningul cancerului mamar cu RMN mamar, începând cu vârsta de 40 de ani, iar femeile ar putea dori să ia în considerare mastectomiile preventive. Persoanele cu o genă ATM mutantă par a fi predispuse și la cancerul tiroidian și pancreatic și sunt mai sensibile la radiații.
PALB2
Mutațiile genei PALB2 sunt, de asemenea, o cauză importantă a cancerului de sân ereditar. Gena PALB2 codifică o proteină care funcționează împreună cu proteina BRCA2 pentru a repara ADN-ul deteriorat din celule. În general, riscul de cancer de sân pe viață cu mutație PALB2 este de până la 58%, deși acest lucru poate varia în funcție de vârstă. Riscul este de 8 ori până la 9 ori mediu pentru femeile cu vârsta sub 40 de ani, dar de aproximativ 5 ori mediu pentru femeile cu vârsta peste 60 de ani.
Dintre cei care poartă o copie a genei, 14% vor dezvolta cancer de sân până la vârsta de 50 de ani și 35% până la vârsta de 70 de ani (mai puțin decât în cazul mutațiilor BRCA).
Persoanele care au o mutație PALB2 și dezvoltă cancer de sân pot avea un risc mai mare de a muri din cauza bolii.
Persoanele care moștenesc 2 copii ale genei mutate PALB2 au un tip de anemie Fanconi caracterizată prin număr foarte scăzut de celule roșii din sânge, globule albe și trombocite.
CHEK2
Gena CHEK2 codifică o proteină care este activată atunci când are loc deteriorarea ADN-ului. De asemenea, activează alte gene implicate în repararea celulelor.
Riscurile pe viață pentru purtătorii de mutații trunchiante CHEK2 sunt de 20% pentru o femeie fără rudă afectată, 28% pentru o femeie cu o rudă de gradul doi afectată, 34% pentru o femeie cu o rudă de gradul I afectată și 44% pentru o femeie cu atât o rudă de gradul I, cât și a doua afectată.
Atât pentru bărbați, cât și pentru femei, gena crește, de asemenea, riscul de cancer de colon și limfom non-Hodgkin.
CDH1
Mutațiile din CDH1 provoacă o afecțiune cunoscută sub numele de sindrom de cancer gastric ereditar.
Persoanele care moștenesc această genă au un risc pe viață de până la 80% pentru dezvoltarea cancerului de stomac și până la 52% pentru dezvoltarea cancerului de sân lobular.
Codurile genetice ale unei proteine (cadherina epitelială) care ajută celulele să se lipească unele de altele (una dintre diferențele dintre celulele canceroase și celulele normale este că celulelor canceroase nu au aceste substanțe chimice de aderență care le fac să se lipească). Cancerele la persoanele care moștenesc această mutație sunt mai susceptibile de a metastaza.
PTEN
Mutațiile genei PTEN sunt una dintre cele mai frecvente mutații genice supresoare tumorale. Codurile genetice ale proteinelor care reglează creșterea celulelor și, de asemenea, ajută celulele să se lipească.
Mutațiile genei par să crească riscul ca celulele canceroase să se desprindă de o tumoare și să facă metastaze. PTEN este asociat cu un sindrom numit sindrom tumoral PTEN hamartom, precum și sindrom Cowden.
Femeile care au o mutație PTEN au un risc pe tot parcursul vieții de a dezvolta cancer de sân cu până la 85% și, de asemenea, au un risc crescut de modificări benigne ale sânului, cum ar fi boala fibrocistică, adenoza și papilomatoza intraductală.
Mutațiile sunt, de asemenea, corelate cu un risc crescut de cancer uterin (și fibroame uterine benigne), cancer tiroidian, cancer de colon, melanom și cancer de prostată.
Simptomele care nu sunt legate de cancer includ dimensiunea mare a capului (macrocefalie) și tendința de a forma tumori benigne cunoscute sub numele de hamartom.
STK11
Mutațiile din STK11 sunt asociate cu o afecțiune genetică cunoscută sub numele de sindrom Peutz-Jegher. STK11 este o genă supresoare tumorale implicată în creșterea celulelor.
În plus față de un risc crescut de cancer de sân (cu un risc pe viață de până la 50%), sindromul prezintă un risc crescut de multe tipuri de cancer, dintre care unele includ cancer de colon, cancer pancreatic, cancer de stomac, cancer ovarian, cancer pulmonar, cancer uterin și multe altele.
Condițiile non-canceroase asociate cu mutația includ polipi necanceroși din tractul digestiv și din sistemul urinar, pistrui pe față și interiorul gurii și multe altele. Depistarea cancerului de sân este adesea recomandată femeilor care încep la 20 de ani și adesea cu RMN cu sau fără mamografii.
TP53
Gena TP53 codifică proteinele care opresc creșterea celulelor anormale.
Aceste mutații sunt extrem de frecvente în cancer, cu dobândit mutațiile genei p53 fiind găsite în aproximativ 50 la sută din tipurile de cancer.
Mutațiile ereditare sunt mai puțin frecvente și asociate cu afecțiuni cunoscute sub numele de sindrom Li-Fraumeni sau sindrom asemănător Li-Fraumeni (care prezintă un risc mai scăzut de cancer). Majoritatea persoanelor care moștenesc mutația dezvoltă cancer până la vârsta de 60 de ani și, pe lângă cancerul de sân, sunt predispuși să dezvolte cancer osos, cancer suprarenalian, cancer pancreatic, colon, cancer hepatic, tumori cerebrale, leucemie și multe altele. Nu este neobișnuit ca persoanele cu mutație să dezvolte mai mult de un cancer primar.
Se crede că mutațiile moștenite ale genei p53 reprezintă aproximativ 1% din cazurile de cancer mamar ereditar. Cancerele de sân asociate cu mutația sunt adesea HER2 pozitive și au un grad tumoral ridicat.
Sindromul Lynch
Sindromul Lynch sau cancerul colorectal ereditar non-polipozic este asociat cu mutații în mai multe gene diferite, inclusiv PMS2, MLH1, MSH2, MSH6 și EPCAM.
PMS2, în special, a fost asociat cu riscul dublu de cancer de sân. Gena funcționează ca o genă supresoare tumorale, codificând o proteină care repară ADN-ul deteriorat.
În plus față de cancerul de sân, aceste mutații prezintă un risc ridicat de cancer de colon, ovar, uter, stomac, ficat, vezică biliară, intestin subțire, rinichi și creier.
Alte mutații
Există mai multe alte mutații genetice asociate cu un risc crescut de a dezvolta cancer de sân și se așteaptă să se descopere mai multe în viitorul apropiat. Unele dintre acestea includ:
- BRIP1
- BARD1
- MRE11A
- NBN
- RAD50
- RAD51C
- SEC23B
- BLM
- MUTYH
Cancerul de sân și testarea genetică
În prezent, testarea este disponibilă pentru mutațiile genei BRCA, precum și pentru mutațiile ATM, CDH1, CHEK2, MRE11A, MSH6, NBN, PALB2, PMS2, PTEN, RAD50, RAD51C, SEC23B și TP53, cu această zonă preconizată să se extindă dramatic în viitorul apropiat.
Cu toate acestea, disponibilitatea acestor teste ridică multe întrebări. De exemplu, cine ar putea avea cancer mamar ereditar și cine ar trebui testat? Ce ar trebui să faceți dacă testați pozitiv pentru una dintre aceste gene?
În mod ideal, orice testare ar trebui făcută numai cu îndrumarea și ajutorul unui consilier genetic. Există două motive pentru aceasta.
Una este că poate fi devastator să afli că ai o mutație care îți poate crește riscul, iar îndrumarea cuiva care este conștient de managementul recomandat și de screening este de neprețuit.
După cum sa menționat anterior, unele mutații conferă un risc ridicat, iar altele un risc mult mai mic. Unele mutații ar putea fi mai îngrijorătoare mai devreme în viață (să zicem, în anii 20), în timp ce altele ar putea să nu necesite screening precoce. Un consilier genetic vă poate ajuta să aflați ceea ce este recomandat în prezent în ceea ce privește screening-ul mutației dvs., luând în considerare orice alți factori de risc pe care i-ați putea avea.
Celălalt motiv pentru care consilierea genetică este atât de importantă este că este posibil să aveți un risc semnificativ de a dezvolta cancer de sân, chiar dacă testele dvs. sunt negative. Mai sunt multe de învățat, iar un consilier genetic vă poate ajuta să analizați istoricul familiei dvs. pentru a vedea dacă este posibil să aveți un risc ridicat în ciuda testelor negative și să planificați screeningul în consecință.
Testarea genetică pentru cancerul de sânSprijin pentru cancerul de sân ereditar
La fel cum persoanele cărora li s-a diagnosticat cancer de sân au nevoie de sprijin, cei care au gene care cresc riscul au nevoie de sprijin. Din fericire, există organizații care se concentrează în mod special pe sprijinirea persoanelor aflate în această situație.
O organizație, FORCE, care este un acronim pentru „Faceți față riscului nostru de cancer împuternicit”, oferă o linie de asistență, un forum de mesaje și informații pentru cei care se confruntă cu cancer ereditar.
Alte organizații și comunități de sprijin sunt disponibile pentru a ajuta oamenii să facă față deciziilor legate de diagnosticul de cancer mamar ereditar.
Termenul „previvor” a fost inventat de FORCE pentru a descrie persoanele care supraviețuiesc unei predispoziții la cancerul de sân. Dacă aceasta este situația cu care vă confruntați, nu sunteți singuri și, folosind hashtagul #previvor, puteți găsi multe altele pe Twitter și alte puncte de socializare.
Un cuvânt de la Verywell
Poate fi copleșitor să aflăm despre numeroasele mutații genetice care cresc riscul cancerului de sân dincolo de mutațiile BRCA, dar aceste „alte” mutații sunt de o importanță semnificativă știind că mutațiile BRCA reprezintă o minoritate relativă a cancerelor de sân familiale. În același timp, știința privind cancerul mamar ereditar este încă la început și există multe de învățat. Dacă sunteți îngrijorat, este posibil să aveți o mutație sau ați învățat că faceți acest lucru, este util să învățați cât de mult puteți. Organizațiile ereditare de cancer, cum ar fi FORCE, nu numai că vă pot oferi informații suplimentare, dar vă pot ajuta să vă conectați cu alții care se confruntă cu o călătorie cu întrebări și preocupări similare.